Etapa de Reacción. Obtención del Biodiésel
De Construmatica
Nota: Este artículo ha sido creado gracias a la Ingenieros Sin Fronteras en el marco del Programa de Afiliados de la Construpedia. El contenido está disponible en el sitio web de Ingeniería Sin Fronteras
|
|---|
La reacción de transesterificación es factible con cualquier alcohol, pero prácticamente sólo el metanol y el etanol se han empleado para este propósito.
El hecho de utilizar exclusivamente el metanol (obteniendo el éster metílico), obedece a su capacidad de reaccionar totalmente con cualquier aceite vegetal de baja acidez.
Las pruebas realizadas con etanol indican mayor dificultad de reacción, el proceso es más complejo, son necesarias condiciones más drásticas de presión y temperatura, el etanol debe ser completamente anhidro, los rendimientos son menores, y el biocombustible que se obtiene es menos estable y resulta ser más costoso, y además se requiere que el aceite sea refinado. Cuando la reacción se realiza con metanol recibe el nombre de metanólisis.
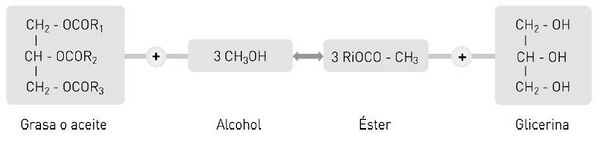
Reacción de transesterificación
La transesterificación con catalizador alcalino, tal como hidróxido de sodio o de potasio, ofrece la ventaja de permitir trabajar en condiciones suaves de bajas temperaturas (aproximadamente la temperatura de ebullición del alcohol). Sin embargo, como los ácidos grasos libres contenidos en el aceite inicial no son esterificados en este proceso, deben ser removidos antes de la transesterificación, o bien esterificar en una etapa de reacción adicional o separar la fracción no esterificable con la fase glicerina.
Los catalizadores ácidos, tales como los ácidos minerales, pueden catalizar tanto la transesterificación como la posterior esterificación de los ácidos grasos libres, pero las condiciones de reacción son más exigentes en cuanto a los reactantes.
Una alternativa es utilizar catalizadores heterogéneos, por ejemplo de intercambio iónico o biocatálisis mediante unas enzimas específicas llamadas lipasas (Mittelbach, 1991).
Se ha comprobado que el efecto de la temperatura en el desarrollo de la reacción es bastante fuerte en los primeros instantes de la reacción, de manera que a temperaturas mayores corresponden velocidades mayores en la formación del producto. Sin embargo, al transcurrir un cierto tiempo, el efecto de la temperatura es prácticamente inapreciable. La reacción es endotérmica, por lo que a mayores temperaturas corresponden velocidades mayores de formación de producto. La temperatura óptima depende del catalizador utilizado.
En la reacción de transesterificación, en teoría se requieren tres moles de alcohol por cada mol de triglicérido, para obtener tres moles de éster y uno de glicerina. En la práctica, se ha comprobado que es necesario adicionar alcohol en exceso para obtener un alto rendimiento del proceso, logrando de esta forma desplazar, casi totalmente, la reacción hacia la formación del éster metílico. La presión y el tiempo de reacción dependen del resto de parámetros seleccionados.
Etapas de transformación de los aceites en biocombustibles
La transformación de los aceites vegetales en biogasóleo por medio de la transesterificación de los mismos, comprende dos etapas principalmente:
La primera es la reacción de transesterificación y la segunda de separación y purificación de los ésteres obtenidos, que son el biogasóleo.
La reacción de transesterificación de los aceites vegetales da como resultado ésteres más glicerina (trialcohol). Los ésteres puros representan el biogasóleo, por esta razón restos de glicerina, glicéridos (mono, di y triglicéridos) y otras sustancias como restos de catalizador, se consideran impurezas que se deben retirar a través de la purificación. Por otra parte se debe tener en cuenta que la glicerina tiene un alto valor añadido en el mercado por su utilidad en industrias como la cosmética y farmacéutica.
Durante la reacción de transesterificación se presentan reacciones secundarias que dan lugar a productos indeseables o que contaminan los ésteres metílicos o biodiésel. Las reacciones secundarias que tiene lugar son principalmente las de formación de jabones, ya sea provenientes de la reacción saponificación de los aceites y/o grasas o de la neutralización de los ácidos grasos libres. La formación de jabones trae como consecuencias negativas, la disminución de la conversión y del rendimiento, la necesidad de etapas posteriores de purificación de los ésteres metílicos y el aumento de la posibilidad de que se presenten emulsiones en las etapas de purificación.